色素瘤切除范围_色素瘤切除手术需要住院吗
*** 次数:1999998 已用完,请联系开发者***
君实生物(01877):特瑞普利单抗二线及以上治疗黑色素瘤获得国家药品...智通财经APP讯,君实生物(01877)发布公告,本公司收到国家药品监督管理局(「国家药监局」)核准签发的《药品补充申请批准通知书》,特瑞普利单抗(商品名:拓益®,产品代号:JS001)用于既往接受全身系统治疗失败的不可切除或转移性黑色素瘤的治疗的适应症获得国家药监局同意,由附...
ˋ﹏ˊ 
ˇ0ˇ 君实生物:特瑞普利单抗二线及以上治疗黑色素瘤获得国家药监局常规...南方财经1月6日电,君实生物公告,公司收到国家药监局核准签发的《药品补充申请批准通知书》,特瑞普利单抗(商品名:拓益®,产品代号:JS001)用于既往接受全身系统治疗失败的不可切除或转移性黑色素瘤的治疗的适应症获得国家药监局同意,由附条件批准转为常规批准。此次常规批准...
˙▽˙ 
君实生物:特瑞普利单抗二线及以上治疗黑色素瘤获国家药监局常规批准金融界1月6日消息,近日,君实生物的特瑞普利单抗(商品名:拓益®,产品代号:JS001)用于既往接受全身系统治疗失败的不可切除或转移性黑色素瘤的治疗适应症,由附条件批准转为常规批准。该药是中国首个批准上市的以PD-1为靶点的国产单抗药物,至今已在全球开展了超过15个适应症的...
君实生物(01877.HK):特瑞普利单抗二线及以上治疗黑色素瘤获得国...君实生物(01877.HK)发布公告,近日,公司收到国家药品监督管理局(以下简称“国家药监局”)核准签发的《药品补充申请批准通知书》,特瑞普利单抗(商品名:拓益®,产品代号:JS001)用于既往接受全身系统治疗失败的不可切除或转移性黑色素瘤的治疗的适应症获得国家药监局同意,由附条...

默沙东PD-1抑制剂可瑞达在华获批黑色素瘤治疗新适应证9月14日,默沙东宣布,其PD-1抑制剂帕博利珠单抗已获得中国国家药品监督管理局批准,用于不可切除或转移性黑色素瘤的一线治疗。此次批准,将产品说明书中黑色素瘤适应证由“帕博利珠单抗适用于经一线治疗失败的不可切除或转移性黑色素瘤的治疗”变更为“帕博利珠单抗适用于...

君实生物:特瑞普利单抗一线治疗黑色素瘤的新适应症上市申请获得受理君实生物公告,收到国家药品监督管理局核准签发的《受理通知书》,特瑞普利单抗用于不可切除或转移性黑色素瘤的一线治疗的新适应症上市申请获得受理。
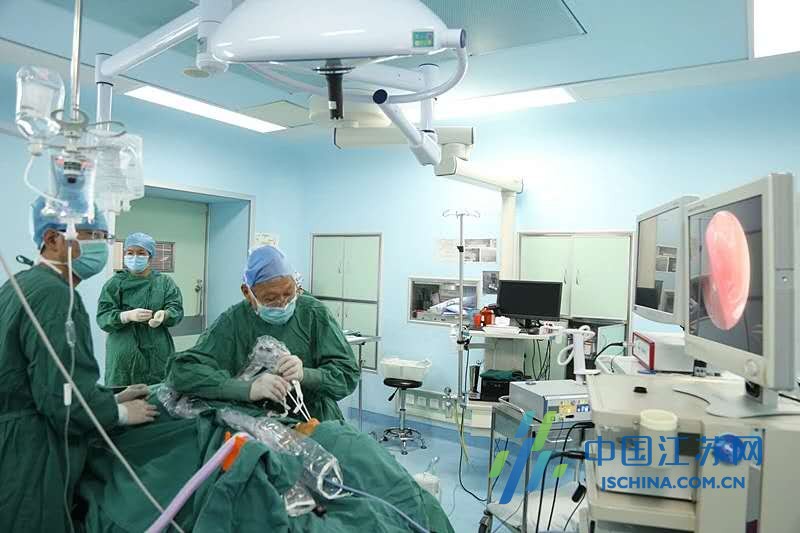
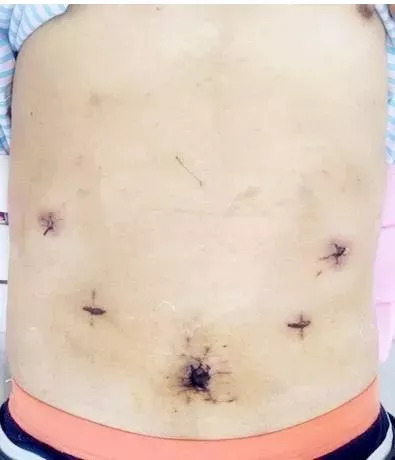
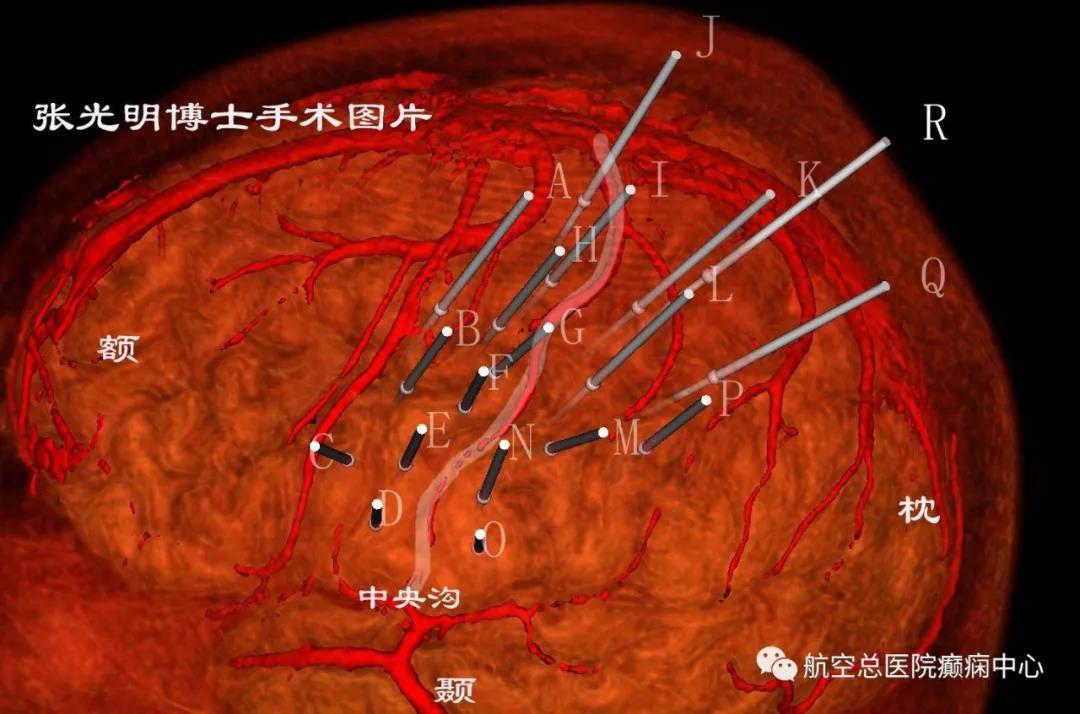
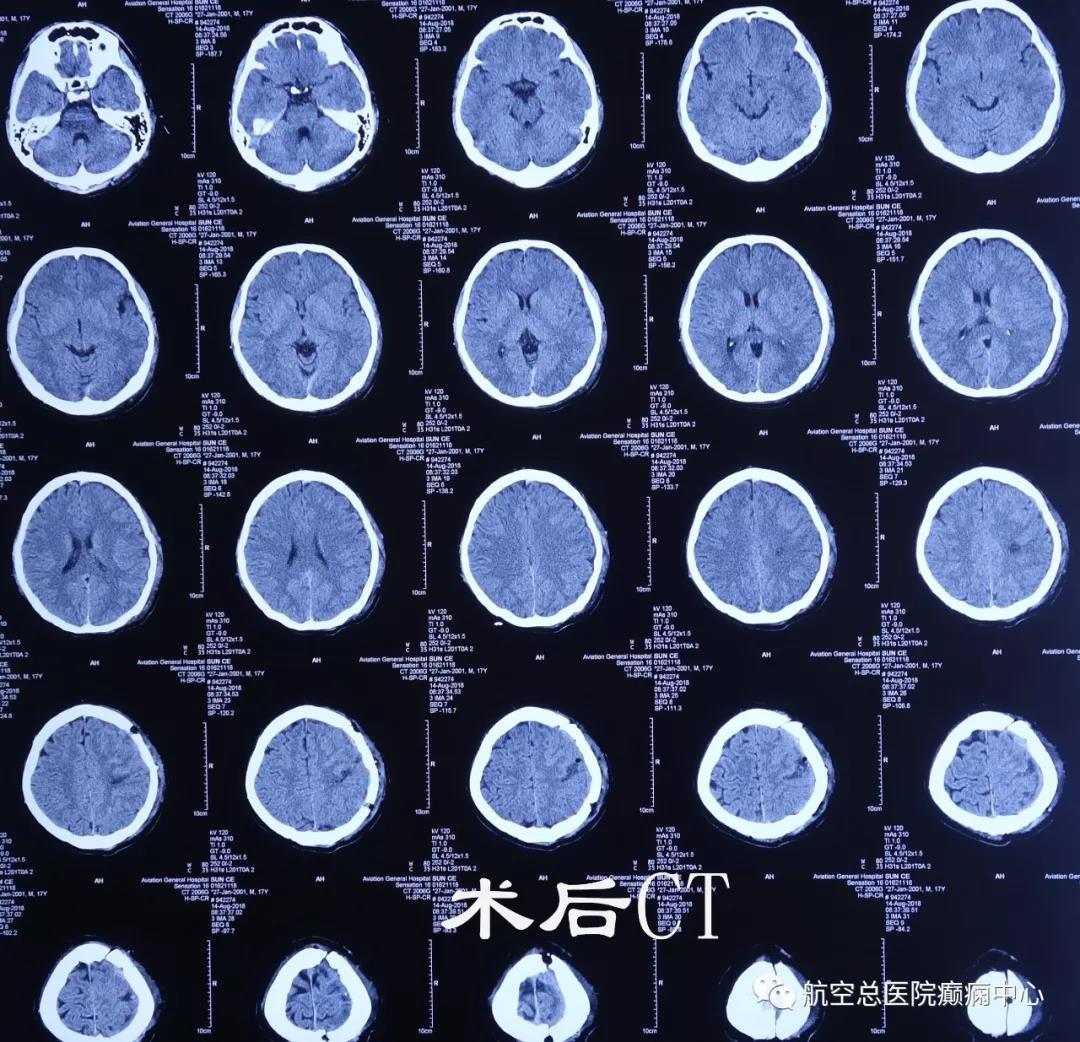
\ _ / 孕期头痛呕吐不止 原是黑色素瘤作祟这一切竟是隐藏在小脑部位的黑色素瘤导致的颅内高压所致。在多学科团队的紧密合作下,王娟成功接受了全麻开颅肿瘤切除手术,术后症状显著缓解,重获安宁。今年26岁的王娟(化名)自幼颜面部便有一块醒目的黑色胎记,因为胎记不痛不痒,对生活没有其他不良影响,也就没有处理。婚后...
≥▽≤ 
君实生物(01877):特瑞普利单抗抗一线治疗黑色素瘤的新适应症上市...用于不可切除或转移性黑色素瘤的一线治疗的新适应症上市申请获得受理。黑色素瘤是恶性程度最高的皮肤癌类型,根据GLOBOCAN 2022发布... 正在进行或已完成的关键注册临床研究在多个瘤种范围内评估特瑞普利单抗的安全性及疗效。截至本公告披露日,特瑞普利单抗的10项适应症已...
●﹏● 
⊙﹏⊙ 君实生物(688180.SH):特瑞普利单抗一线治疗黑色素瘤的新适应症上市...君实生物(688180.SH)公告,近日,公司收到国家药品监督管理局核准签发的《受理通知书》,特瑞普利单抗(商品名:拓益®,产品代号:JS001)用于不可切除或转移性黑色素瘤的一线治疗的新适应症上市申请获得受理。

Moderna(MRNA.US)/默沙东(MRK.US)公布黑色素瘤组合疗法中期试验...周一,Moderna(MRNA.US)与默沙东(MRK.US)在美国临床肿瘤学会(ASCO)年会上公布了一项评估治疗致命皮肤癌的组合疗法在近三年时间里取得的积极数据。据悉,在一项针对经手术切除高风险黑色素瘤(III/IV期)患者的中期试验中,Moderna旗下的个体化新抗原疫苗mRNA-4157(V940)与...
i7加速器部分文章、数据、图片来自互联网,一切版权均归源网站或源作者所有。
如果侵犯了你的权益请来信告知删除。邮箱:xxxxxxx@qq.com
上一篇:色素瘤切除手术需要住院吗
下一篇:色素瘤切除还会长吗





